
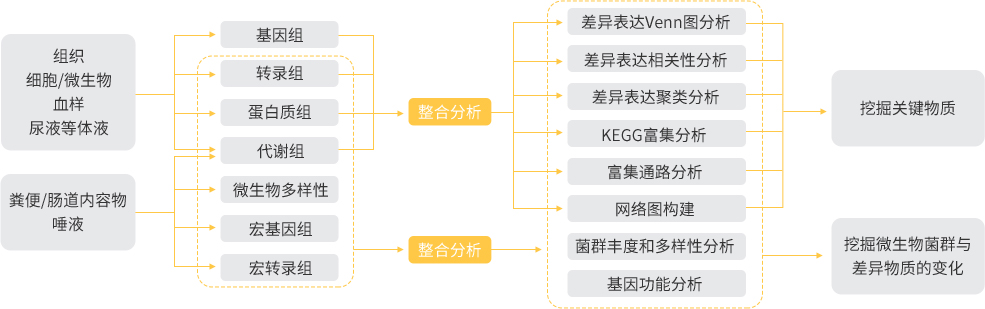
多组学(Multi-Omics):探究生物系统中多种物质之间相互作用的方法,包括基因组学、表观基因组学、转录组学、蛋白质组学、代谢组学、微生物组学等,这些物质共同影响生命系统的表型、性状等。系统生物学研究时代,生物学现象复杂多变,基因表达调控复杂多样,单纯用单一组学研究结论往往不够全面,采用多组学联合分析可以实现蛋白 / 转录及代谢物的全谱分析,实现从“因”和“果”两个方向探究生物学问题,相互间的验证作用更明显还可以阐述分子调控 - 表型间的关联机制,筛选出重要代谢通路或基因、蛋白、代谢物进行实验分析和研究。
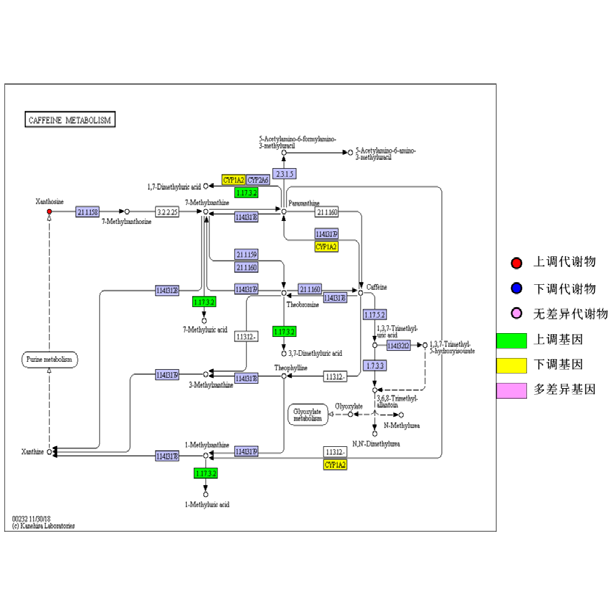 整合代谢通路图
整合代谢通路图 关联热图
关联热图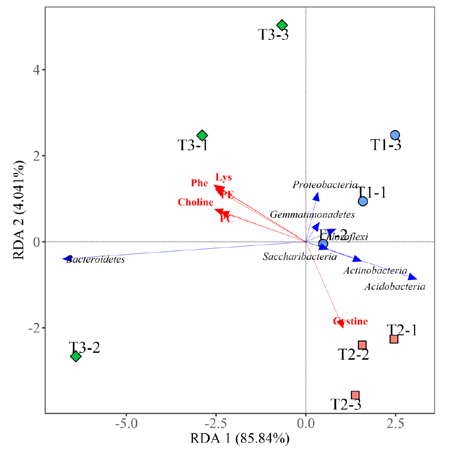 冗余分析 ( 响应变量和解释变量之间多元多重线性回归关系 )
冗余分析 ( 响应变量和解释变量之间多元多重线性回归关系 ) ROC 曲线 ( 标记物对不同组别的 识别分类能力 )
ROC 曲线 ( 标记物对不同组别的 识别分类能力 ) 基于代谢通路的网络关联图
基于代谢通路的网络关联图 单个样本中代谢物和蛋白关联散点图
单个样本中代谢物和蛋白关联散点图期刊:Small 影响因子:11.459 发表时间:2020年6月 发表单位:复旦大学
免疫治疗和免疫检查点阻断疗法是非常有前景的治疗手法。然而,由于肿瘤微环境的复杂性和宿主免疫系统的钝化,免疫治疗策略在许多癌症的抗肿瘤反 应中仍然存在局限性。通过其他免疫原性疗法与检查点阻断疗法联合可提供非炎症肿瘤的免疫应答率。因此,开发有效的抗肿瘤诱导和免疫调节的新途径和策略,对免疫治疗具有重要意义。
铁死亡是近年来发现的一种新的细胞死亡形式,它能有效抑制肿瘤生长,并适当产生免疫原性,而具有免疫逃避和肿瘤靶向能力的血小板膜包衣的纳米颗粒可以最大限度将诱导铁死亡的药物递 送到肿瘤,从而在肿瘤转移的铁死亡治疗中发挥出完全的潜力。作者发明了一种血小板膜包衣载有柳氮磺吡啶的介孔磁性纳米颗粒 (Fe3O4-SAS@PLT) 诱导铁死亡和 PD-1 免疫检查点阻断疗法结合的铁死亡增强肿瘤免疫治疗策略。
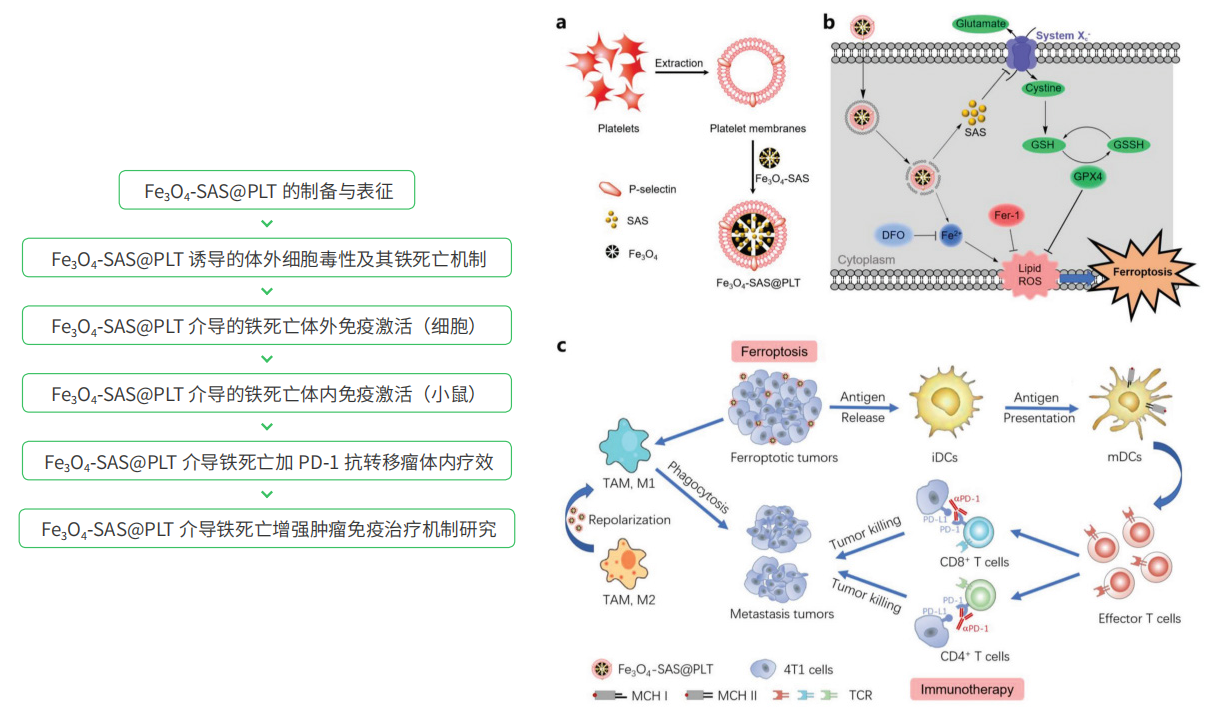 图 1 血小板膜修饰磁性纳米颗粒增强肿瘤免疫治疗的示意图
图 1 血小板膜修饰磁性纳米颗粒增强肿瘤免疫治疗的示意图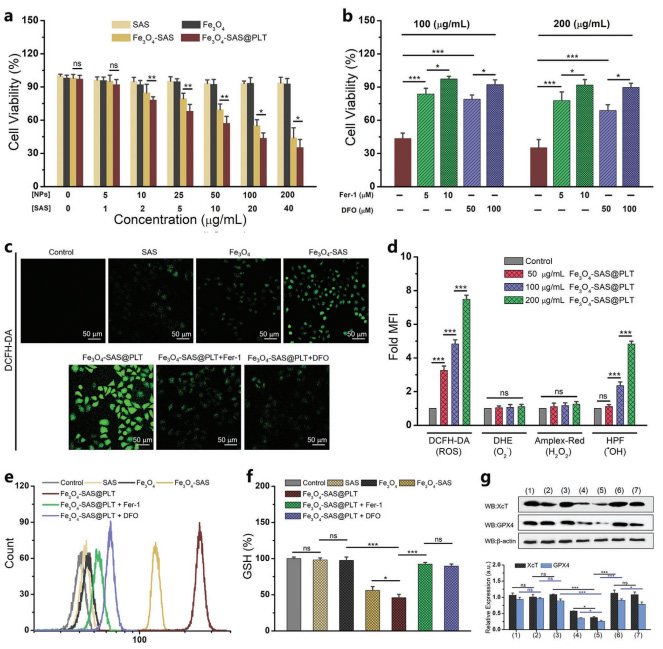 图 2 Fe3O4-SAS@PLT 体外细胞毒性及铁死亡机制的研究
图 2 Fe3O4-SAS@PLT 体外细胞毒性及铁死亡机制的研究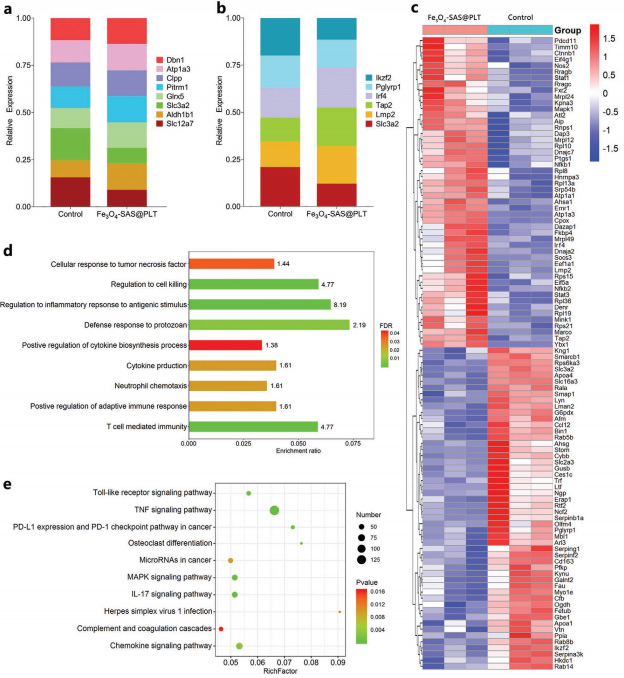 图 3 Fe3O4-SAS@PLT 介导的上铁死亡增强抗肿瘤免疫反应的机制
图 3 Fe3O4-SAS@PLT 介导的上铁死亡增强抗肿瘤免疫反应的机制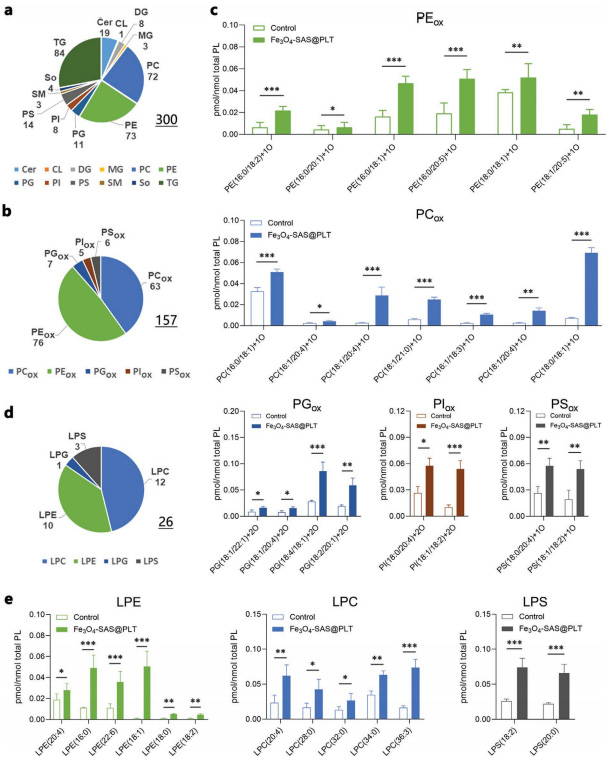 图 4 Fe3O4-SAS@PLT 介导的铁死亡体内免疫激活
图 4 Fe3O4-SAS@PLT 介导的铁死亡体内免疫激活本研究发明了一种仿生磁性纳米颗粒 (Fe3O4-SAS@PLT) 介导铁死亡和提高肿瘤免疫治疗疗效。有血小板的自我识别特性,Fe3O4-SAS@PLT纳米粒表现出有效的免疫逃逸和靶向富集肿瘤转移靶点。Fe3o4-SAS@PLT 纳米粒不仅可以通过抑制系统 XcT通路诱 导铁依赖的铁死亡发生,而且可以诱导有效的免疫反应,提高 PD-1 阻断疗法的体内治疗效果。相比于单一治疗方式,Fe3o4-SAS@PLT 介导的铁死亡联合免疫治疗有效抑制了肿瘤的生长和转移,提供了一种临床适用的协同免疫治疗的新途径。
Jiang Qin,Wang Kuang,Zhang Xingyu et al. Platelet Membrane-Camouflaged Magnetic Nanoparticles for FerroptosisEnhanced Cancer Immunotherapy.[J] .Small, 2020, 16: e2001704
期刊:Movement Disorders 影响因子:8.679 发表时间:2020年 发表单位:不列颠哥伦比亚大学
帕金森氏病的特征是胃肠道疾病的高负担,特别是便秘和结肠传输时间缩短,以及肠道微生物群的改变。微生物群产生的各种代谢物与宿主健康有着广泛的关系。帕金森病的微生物群组成和代谢与胃肠功能的关系尚不清楚。本研究的 目的是评估微生物群组成、粪便稠度、便秘之间的关系,以及帕金森病的微生物代谢产物,以便更好地了解肠道微生物及代谢物与帕金森的相关性。
300 名受试者(197 名帕金森病患者和 103 名对照者)被纳入这项队列研究。参与者提供粪便样本用于微生物群测序(n=300),血清用于非靶向代谢组学(n=125)。收集帕金森患者运动时和非运动状态时的症状、药物、饮食和人口统计。
在帕金森病患者中观察到了显著的微生物群落分类差异,即使在控制胃肠功能的情况下也是如此。帕金森氏菌群的特点是碳水化合物发酵和丁酸盐合成能力降低,蛋白水解发酵和有害氨基酸代谢物(包括对甲酚和苯乙酰基谷胱甘肽)的产生增加。分类学改 变和蛋白水解代谢产物升高与大便稠度(结肠转运时间的代表)和便秘密切相关。
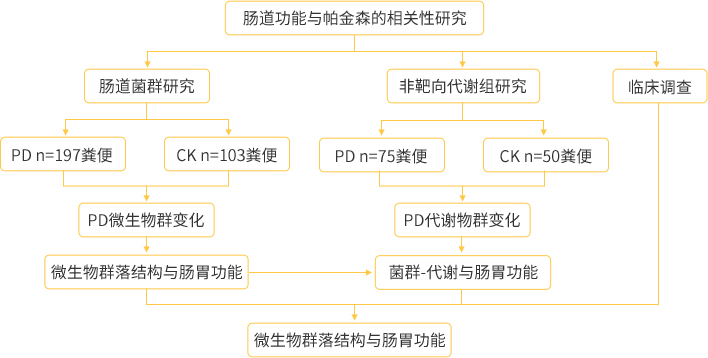
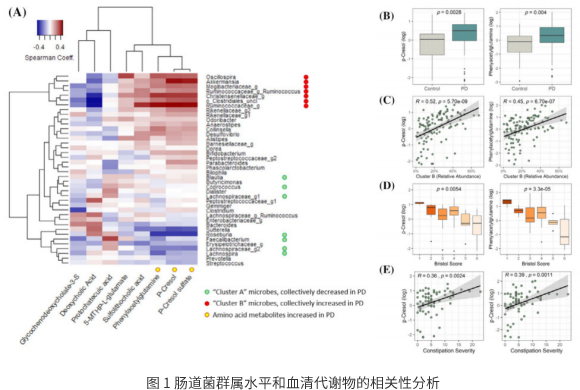
帕金森氏菌群的组成和代谢改变与肠道功能密切相关,提示细菌代谢和肠道健康下降之间可能存在的联系。对帕金森氏症患者体内高水平的有害蛋白水解微生物代谢产物的系统检测表明,微生物降解作用有助于疾病的病因和病理生理学研究。
Cirstea Mihai S,Yu Adam C,Golz Ella et al. Microbiota Composition and Metabolism Are Associated With Gut Function in Parkinson's Disease.[J] .Mov. Disord., 2020, 35: 1208-1217
期刊:Molecular Metabolism 影响因子:6.448 发表时间:2020年 发表单位:罗马大学
肠道微生物群的代谢影响在心脏代谢性疾病的发病中起着关键作用。抗生素影响肠道细菌多样性,长期使用已被确定为动脉粥样硬化驱动事件的独立危险因素。本研究旨在探讨抗生素引起的肠道菌群失调与代谢途径对动脉粥样硬化的影响之间的相互作用硬化发展。
在载脂蛋白 E 基因敲除小鼠模型中,我们将口服抗生素与不同饮食相结合,通过整合肠道微生物群与动脉粥样硬化病变的发展交叉组学方法包括血清代谢组学和盲肠16SrRNA 靶向基因组测序。我们进一步研究了颈动脉粥样硬化患者与心血管疾病对照组的对比风险。
这里,我们发现抗生素引起的动脉粥样硬化增加与肠道多样性的丧失和微生物代谢功能的改变有关,并对宿主血清代谢组产生重大影响。由抗生素调节并与动脉粥样硬化相关的途径包括色氨酸减少和脂质代谢紊乱。这些途径与抗生素在肠道中减少某些类杆菌和梭状芽孢杆菌有关。动脉粥样硬化患者表现出与抗生素诱导的小鼠相似的代谢特征模型。

综上所述,这项工作提供了肠道微生物群和宿主代谢之间复杂相互作用的见解。我们的数据强调,抗生素对肠道菌群的有害影响与除经典危险因素外的促动脉粥样硬化代谢表型有关。
Kappel B A , Angelis L D , Heiser M , et al. Cross-omics analysis revealed gut microbiome-related metabolic pathways underlying atherosclerosis development after antibiotics treatment[J]. Molecular Metabolism, 2020
Copyright © 2015-2023 苏州帕诺米克生物医药科技有限公司 版权所有